Ионная связь проявляется тогда, когда электроотрицательность элементов резко отличаются между собой (по шкале Полинга Δχ > 1,7), а это происходит при взаимодействии ионов, образованных из атомов элементов, характеризующихся существенно отличными химическими свойствами.
Ионная связь — это электростатическое притяжение между разноименно заряженными ионами, которые образованы в результате полного смещения общей электронной пары от атома одного элемента к атому другого элемента.
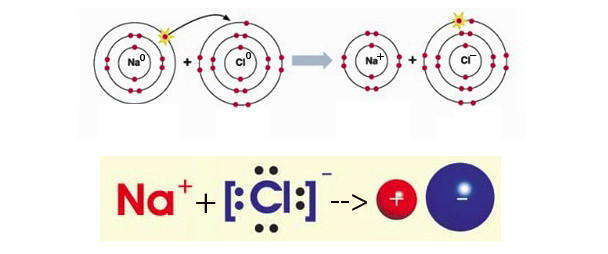
В зависимости от индивидуальных свойств у атомов одних элементов преобладает тенденция к потере электронов с преобразованием в положительно заряженные ионы (катионы ), а атомы других элементов, наоборот, стремятся приобрести электроны, превращаясь при этом в отрицательно заряженные ионы (анионы ), как это происходит с атомами обычного металла натрия и типичного неметалла хлора.
Способность элементов образовывать простые ионы (то есть исходящие от одного атома) обусловлена электронной конфигурацией их изолированных атомов, а также величинами электроотрицательности, энергий ионизации и сродства к электрону (минимальная энергия, необходимая для удаления электрона из соответствующего отрицательного иона на бесконечное расстояние). Понятно, что катионы легче образуются атомами элементов с малыми энергиями ионизации — щелочных и щелочно-земельных металлов (Na, К, Cs, Rb, Ca, Ba, Sr и т.д.). Образование же простых катионов других элементов менее вероятно, поскольку это связано с расходом большой энергии на ионизацию атома.
Простые анионы легче образуются р-элементами седьмой группы (Cl, Br, I) вследствие их высокого сродства к электрону. Присоединение по одному электрону к атомам О, S, N сопровождается выделением энергии. А присоединение других электронов с образованием многозарядных простых анионов энергетически невыгодно.
Поэтому соединения, состоящие из простых ионов, немногочисленны. Они легче образуются при взаимодействии щелочных и щелочно-земельных металлов с галогенами.
Характеристики ионной связи
1. Ненаправленность. Электрические заряды ионов обусловливают их притяжение и отталкивание и в целом определяют стехиометрический состав соединения. Ионы можно представить как заряженные шарики, силовые поля которых равномерно распределяются во всех направлениях в пространстве. Поэтому, например, в соединении NaCl ионы натрия Na+ могут взаимодействовать с ионами хлора Cl- в любом направлении, привлекая определенное их число.
Ненаправленность — это свойство ионной связи, обусловленной способностью каждого иона притягивать к себе ионы противоположного знака в любом направлении.
Итак, ненаправленность объясняется тем, что электрическое поле иона имеет сферическую симметрию и уменьшается с расстоянием по всем направлениям, поэтому взаимодействие между ионами осуществляется независимо от направления.
2. Ненасыщенность. Понятно, что взаимодействие двух ионов противоположного знака не может привести к полной взаимной компенсации их силовых полей. Поэтому ион с определенным зарядом сохраняет способность притягивать другие ионы противоположного знака по всем направлениям. Количество таких «привлеченных» ионов ограничивается только их геометрическими размерами и силами взаимного отталкивания.
Ненасыщенность — это свойство ионной связи, которое проявляется в способности иона, который имеет определенный заряд, присоединять любое количество ионов противоположного знака.
3. Поляризация ионов. При ионной связи каждый ион, будучи носителем электрического заряда, является источником силового электрического поля, поэтому при близком расстоянии между ионами они взаимно влияют друг на друга.
Поляризация иона — это деформация его электронной оболочки под воздействием электрического силового поля другого иона.
4. Поляризуемость и поляризующая способность ионов. При поляризации самому сильному смещению подвергаются электроны внешнего слоя. Но при действии одного и того же электрического поля различные ионы деформируются в неодинаковой степени. Чем слабее связаны внешние электроны с ядром, тем легче происходит поляризация.
Поляризуемость — это относительное смещение ядра и электронной оболочки в йоне при воздействии силового электрического поля другого иона. Поляризующая способность ионов — это их свойство оказывать деформирующее действие на другие ионы.
Поляризующая способность зависит от заряда и размера иона. Чем больше заряд иона, тем сильнее его поле, то есть наибольшую поляризующей способностью обладают многозарядные ионы.
Свойства ионных соединений
При обычных условиях ионные соединения существуют в виде твердых кристаллических веществ, которые имеют высокие температуры плавления и кипения, поэтому считаются нелетучими. Например, температуры плавления и кипения NaCl составляют соответственно 8010С и 14130С, CaF2 — 14180С и 25330C. В твердом состоянии ионные соединения не проводят электрический ток. Они хорошо растворяются в воде и слабо или совсем не растворяются в неполярных растворителях (керосин, бензин). В полярных растворителях ионные соединения диссоциируют (распадаются) на ионы. Это объясняется тем, что ионы имеют более высокие энергии сольватации, которые способны компенсировать энергию диссоциации на ионы в газовой фазе.
