Согласно современным представлениям основные положения атомно-молекулярной теории сводятся к следующим тезисам:
- Частицы веществ непрерывно движутся.
- Между частицами вещества действуют силы взаимного притяжения и отталкивания.
- Между составляющими частицами вещества существуют расстояния, размер которых зависит от агрегатного состояния.
- Молекулы состоят из атомов.
- Молекулы сохраняются при физических явлениях и разрушаются во время химических реакций.
- Атомы во время химических процессов остаются неделимыми, но перегруппировываются, в результате чего образуются новые соединения.
- Разнообразие веществ в природе обусловлена различными сочетаниями атомов, благодаря чему могут возникать вещества с молекулярным или немолекулярным строением.
Важнейшие понятия атомно-молекулярного учения
Согласно атомно-молекулярному учению, главными объектами химии являются атомы, молекулы, химические элементы, простые и сложные вещества.
Атом
Атомы — химически неделимые частицы, которые сохраняются при химических реакциях, но при этом частично может меняться строение электронной оболочки. Однако атомы разрушаются в процессе ядерных реакций.
Атом — это наименьшая, химически неделимая, электронейтральная частица элемента, которая состоит из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
Атом — это система, состоящая из ядра и электронной оболочки. В состав атомного ядра, радиус которого в 10000 раз меньше (10-14 -10-15 м) радиуса атома (~ 10-10 м), входят ядерные частицы нуклоны.
Нуклоны — это положительно заряженные протоны и электронейтральные нейтроны. Электронная оболочка, размер которой определяет радиус всего атома — это совокупность электронов. Положительный заряд ядра определяется количеством протонов и равна по абсолютной величине отрицательному заряду электронной оболочки, который соответствует количеству электронов. Благодаря равенству по абсолютной величине зарядов протонов и электронов, атом электронейтрален. Протоны, нейтроны и электроны объединяются общим названием — субатомные частицы.
Массы протона и нейтрона практически одинаковы, а масса электрона в 1836 раз меньше, поэтому вся масса атома фактически сосредоточена в его ядре. По этой причине плотность вещества в ядре фантастически велика — порядка 1013 -1014 г / см3 . Массы атомов различных элементов колеблются от 1,67 · 10-27 кг (атом водорода) до 4,42 · 10-25 кг (атом мейтнерия — элемента № 109).
Количественными характеристиками атома является заряд ядра и относительная атомная масса Аr . Эти величины указываются в периодической системе элементов.
Заряд ядра атома равен порядковому номеру элемента (закон Мозли).
Поскольку массы атомов очень малы, в химии внедрена внесистемная единица измерения, называемая атомной единицей массы (а.е.м.) и равна одной двенадцатой массы атома изотопа углерода-12 (m (атома 12 С) = 19,92 · 10-27 кг):
Относительная атомная масса Аr — это физическая величина, равная отношению средней массы атома элемента к одной двенадцатой массы атома изотопа углерода-12:
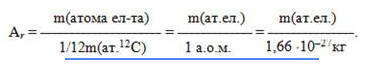
В системе измерений СИ Аr — безразмерная величина. Внесистемная единица измерения относительной атомной массы — а.е.м. Абсолютная масса атома равна произведению его относительной атомной массы на 1/12 массы атома углерода — 12 , например
m (ат.О) = А r (О) · 1,66 · 10— 27 = 16 · 1,66 · 10— 27 = 26,56 · 10— 27 кг.
Атом носителем химических свойств элемента . Вместе с этим у атомов одного элемента могут быть разные массы вследствие явления изотопии , при котором атомы одного элемента содержат одинаковое количество протонов в ядре, но разное количество нейтронов, что сказывается на их массе .
Молекула
Молекулы — это реально существующие природные объекты, что подтверждается многими экспериментально доказанными фактами.
Молекула — это наименьшая частица вещества, которая способна самостоятельно существовать и имеет все химические свойства вещества.
Как материальные частицы молекулы имеют размеры и массы. Размеры молекул колеблются в пределах 10-10 — 10-7 м. Масса отдельной молекулы чрезвычайно мала. Так, масса молекулы воды составляет 2,895×10-26 кг.
Молекула сохраняет химические свойства вещества. Известно, что вещество характеризуется определенными физическими и химическими свойствами. Физические свойства — это агрегатное состояние, плотность, температуры кипения и плавления, электропроводность, диэлектрическая проницаемость, цвет, запах, вкус и тому подобное. Понятно, что перечисленные свойства веществ могут быть присущи не одной молекуле, а достаточно большой их совокупности. Однако молекула имеет и собственные физические свойства: дипольный и магнитный моменты, способность к поляризации и тому подобное. А химические свойства вещества (способность вступать в химическое взаимодействие с другими веществами) в полной мере относятся и каждой отдельной молекуле.
Молекулы состоят из атомов, которые соединены между собой химическими связями в определенной последовательности и определенным образом ориентированы в пространстве. Количество атомов в молекуле колеблется от двух (Н2, О2, НСl) до нескольких тысяч (витамины, гормоны, белки). Атомы благородных газов (He, Ne, Ar, Kr, Xe, Rn) иногда называют одноатомными молекулами. Состав молекулы — важнейшая характеристика молекулы и вещества — описывается химическими формулами.
Между молекулами есть расстояния, обусловленные агрегатным состоянием вещества: в газах они составляют 10-8 — 10-7 м, в твердых телах — примерно 10-10 м.
При физических явлениях молекулы сохраняются, а при химических превращениях — разрушаются, образуя новые вещества.
Количественной характеристикой молекулы является относительная молекулярная масса Мr .
Относительная молекулярная масса Мr— это отношение средней массы молекулы вещества к 1/12 массы атома углерода-12.
В системе СИ относительная молекулярная масса Mr — безразмерная величина, а внесистемной единицей ее измерения является а.е.м.
Относительная молекулярная масса Мr равна сумме относительных атомных масс Аr элементов, входящих в состав молекулы, с учетом количества атомов каждого элемента , например:
M r (SO 2 ) = A r (S) + 2 A r (O) = 32 + 2 · 16 = 64 а.е.м.
Абсолютная масса молекулы определяется как произведение Мr на атомную единицу массы:
m (молекулы SO 2 ) = M r (SO 2 ) · 1,66 · 10 — 27 = 64 · 1,66 · 10 — 27 = 1,06 · 10 — 25 кг.
Молекулярное строение имеют органические соединения и часть неорганических веществ, но большинство неорганических веществ состоит из ионов, в которых носителями химических свойств является условные частицы — ассоциаты ионов. Поэтому к веществам ионной строения невозможно применять понятие «молекула» так же как и к металлов и их сплавов, кристаллическая решетка которых имеет свои специфические особенности. Таким образом, с современной точки зрения молекула — это наименьшая электронейтральна замкнутая совокупность атомов, образует определенную структуру с помощью химических связей.
Химический элемент
Сейчас известно 118 химических элементов: из них 89 обнаружены в природе, а другие получены искусственно при проведении ядерных реакций.
Химический элемент — это вид атомов с одинаковым зарядом ядра.
Каждый элемент имеет свое название и символ. Названия элементов с порядковыми номерами 104-109 утверждены советом IUPAC (1997.) Позже были названы другие элементы. Теперь элемент №104 имеет следующие название и символ: Резерфорд Rf, №105 — Дубний Db, №106 — Сиборгий Sg, №107 — Борий Bh, элемент №108 — Хассий Hs, №109 — Мейтнерий Mt, №110 — Дармштадтий Ds. Химические элементы №№111-118 еще не получили официальных названий, поэтому их пока называют по порядковым номерам, например: №111 — Унунуний Uuu (один, один, один) №112 — Унунбий Uub (один, один, два) и т.д.
Химический символ означает, во-первых, название элемента, во-вторых, — один атом этого элемента при записях формул химических реакций.
Носителем свойств химических элементов является атом. Входя в состав различных веществ, атомы каждого элемента придают им определенных свойств. Так, вещества NaCl, Na2S, Na2O имеют некоторые общие свойства благодаря наличию иона Na+ , но также и различия за счет ионов Cl— , S2 , O2.
Основной количественной характеристикой элемента является заряд ядра его атомов Z , совпадающей с порядковым номером элемента. В природе отсутствуют различные химические элементы, которые должны одинаковый заряд ядра, поэтому можно однозначно определить элемент с зарядом ядра его атома. Относительная атомная масса Аr тоже в определенной степени может служить количественной характеристикой элемента, но не исчерпывающей, так как по величине Аr невозможно определить элемент. Существуют атомы различных элементов с одинаковыми Аr — так называемые изобары. С другой стороны, как уже упоминалось, существуют атомы одного и того же элемента с различными Аr — изотопы.
Формулы изотопов конечно записывают с помощью символа химического элемента, отметив заряд ядра (слева снизу) и массового числа (слева сверху). Исключением являются изотопы элемента водорода, для которых наряду с традиционной символикой допускаются и индивидуальные названия и обозначения.
Простые и сложные соединения
Поскольку вещество — это любая совокупность атомов или молекул, то по составу все соединения можно разделить на простые и сложные.
Простыми веществами называются вещества, которые состоят из атомов одного элемента; простые вещества — это форма существования химического элемента в свободном состоянии.
Насчитывается более 500 простых веществ, а элементов известно всего 118. Такое расхождение объясняется явлением под названием аллотропия.
Аллотропия — это способность элемента образовывать несколько простых, отличающихся по свойствам веществ, которые называются аллотропными модификациями, или алотропамы.
Простые вещества могут иметь молекулярное и немолекулярное строение — атомное или металлическое. Молекулярное строение присуще кислороду, галогенам; атомное — благородным газам, алмазу, графиту; металлическое — металлам в разном состоянии.
Сложными веществами называются вещества, содержащие атомы различных элементов, то есть это форма существования элементов в связанном состоянии.
Сложные вещества могут иметь как молекулярное строение (Н2S, CH4, HCl, H2O), так и немолекулярное: ионное (NaCl, Na2O, NaOH) или металлическое (Fe3C — карбид железа).
Химические реакции, их классификация
Химическими реакциями являются процессы, при которых изменяется состав соединений вследствие разрушения связей в одних веществах и образования новых соединений.
Химические реакции — это явления, при которых происходят превращения одних веществ в другие без изменения состава атомных ядер.
Для условного записи химических реакций применяют уравнения химических реакций, где в левой части указывают формулы исходных веществ, а в правой — конечных продуктов, образовавшихся в результате реакции Перед формулами всех веществ проставляют необходимые стехиометрические коэффициенты — числа, с помощью которых сравнивают количества атомов каждого элемента слева и справа.
Итак, уравнение химической реакции — условный запись, в которой с помощью химических формул соединений и стехиометрических коэффициентов отмечают состав и количество исходных веществ и продуктов реакции .
Химические реакции всегда сопровождаются физическими эффектами, которые подтверждают протекание реакции. Визуальными признаками химических реакций обычно является выделение газа, выпадение осадка, изменение окраски реакционной среды или тепловой эффект.
Для химических реакций, проходящих между неорганическими реагентами, чаще всего используются такие классификации:
- По признаку изменения количества и состава исходных веществ и конечных продуктов все реакции делятся на типы:
- реакции разложения, в которых из одного сложного вещества образуется несколько продуктов. В общем виде:
- A → B + C+ DA→B+C+D
- реакции соединения , в которых из нескольких веществ относительно простого состава образуется одна сложное вещество:
- A + B + C→ DA+B+C→D
- реакции замещения, в которых простое вещество замещает составную часть сложного вещества, в результате чего образуются другие простая и сложная вещества: A + B C→ A B + CA+BC→AB+C.
- реакции обмена, в которых молекулы сложных веществ обмениваются своими составными частями: A B + CD → A D + B CAB+CD→AD+BC.
- По признаку изменения валентных состояний атомов выделяют:
- окислительно-восстановительные реакции, при которых происходит изменение степеней окисления у атомов одного или нескольких исходных веществ. Этот тип реакций подробно будет рассматриваться позже, а здесь мы ограничимся только примером окислительно-восстановительной реакции с указанием степеней окисления:
- реакции невалентных преобразований, в процессе которых меняется только состав веществ, а электронные оболочки отдельных атомов остаются неизменными, а значит и степени окисления в атомах всех элементов не изменяются. Типичными случаями реакций невалентных преобразований являются реакции обмена, а также некоторые реакции соединения и разложения.
- В зависимости от направления течения реакции делятся на:
- оборотные, при которых протекание реакций происходит как в прямом, так и в обратном направлении. Следует помнить, что при записи оборотных реакций вместо знаков равенства или стрелочки (= или →→) Ставят две стрелки, направленные в противоположные стороны (↔↔ или ⇔⇔).
- необратимые, идущие в одном направлении до полного расходования хотя бы одного из реагентов. Как правило, необратимые реакции имеют одну из следующих признаков: а) продукты, получаемые, выходят из реакционной среды в виде осадка или газа; b) образуются малодиссоциированные соединения (то есть слабые электролиты: вода, слабая кислота или слабое основание) с) выделяется большое количество теплоты (горение, взрыв).
- По агрегатному или фазовым состоянием реакции делятся на следующие группы:
- гомогенные, при которых вещества, содержащиеся в системе, не отделяются друг от друга поверхностью раздела фаз;
- гетерогенные, характеризующихся наличием поверхности раздела фаз, то есть хоть одно соединение находится в другом агрегатном состоянии, чем остальные веществ.
- По характеру энергетического воздействия выделяют следующие реакции:
- термохимические, которые сопровождаются тепловым эффектом, то есть энергия подводится или отводится в форме теплоты. По знаку тепловых эффектов реакции делятся на следующие типы:
- экзотермические, сопровождающиеся выделением теплоты;
- эндотермические, при которых теплота поглощается;
- фотохимические, которые происходят под действием света сопровождаются излучением световой энергии
- электрохимические, протекающих под действием электрической энергии или сами являются источником электрического тока. Электрохимические реакции происходят в гальванических элементах, при электролизе и при коррозии металлов.
- термохимические, которые сопровождаются тепловым эффектом, то есть энергия подводится или отводится в форме теплоты. По знаку тепловых эффектов реакции делятся на следующие типы:
- В зависимости от природы реагирующих частиц реакции могут быть:
- молекулярными, при которых взаимодействие между веществами проходит результате столкновения отдельных молекул реагирующих веществ;
- ионными, протекающих при взаимодействии между ионами;
- радикальными, при которых одной из взаимодействующих частиц является радикал. Радикалы при записи обозначают с помощью точки рядом с формулой (∙∙).
- При наличии постороннего влияния на скорость реакции они делятся на:
- каталитические, протекающих в присутствии катализаторов — специальных веществ, которые ускоряют реакцию;
- некаталитические, в которых ускоряющий влияние катализатора отсутствует.
Одна и та же реакция в зависимости от признака рассматриваемого может классифицироваться по-разному. Например, синтез NH3 с N2 и H2 в присутствии железного катализатора является реакцией сообщения и одновременно относится к окислительно-восстановительным, гомогенным, молекулярным, каталитическим, термохимическим и оборотным реакциям.

Если исходить из общепринятого сегодня строения атомов из электронов, протонов и нейтронов, то всё научное сообщество не сможет объяснить – на основании чего протоны, нейтроны и электроны создают атомы с разными их количествами. Все атомы излучают конкретный спектр ЭМ волн. При этом чем больше длина волны в спектре конкретного элемента, тем больше размер его атома и атомный вес, тем большее количество энергии заключается в атоме. Поэтому каждый атом выделяет конкретный спектр ЭМ волн, из которых он образуется и состоит. То есть атомы и клетки формируются из ЭМ волн при наличии необходимых и достаточных условий. Только для образования атомов и клеток ЭМ волны из прямолинейного движения переходят во вращательное, образуя магнитную оболочку атомов и клеток.